概要
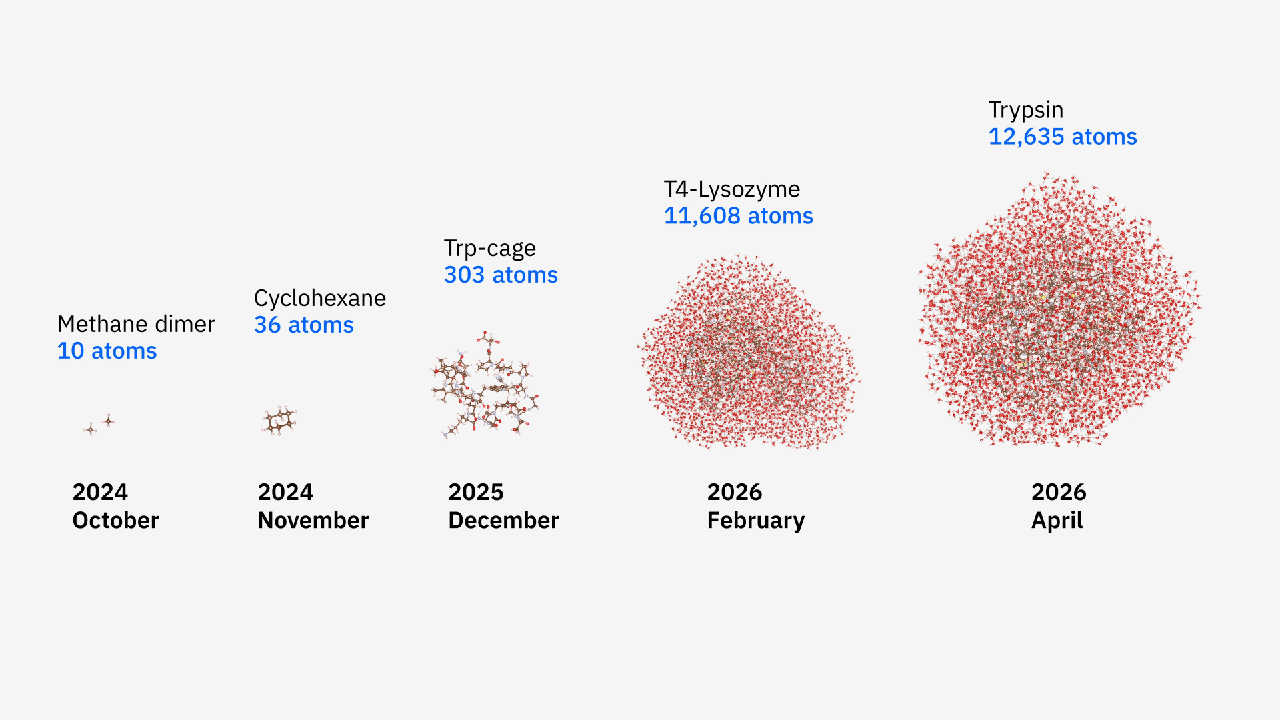
クリーブランドクリニック、理化学研究所、IBMの研究者チームが、量子中心型スーパーコンピューティング(QCSC)フレームワークを用いて、これまでで最大の12,635原子からなるタンパク質-リガンド複合体の電子構造シミュレーションに成功しました。この成果は、T4-リゾチームやトリプシンなどのタンパク質を水溶液中で高精度にモデリングしたもので、以前の結果と比較してシステムサイズが40倍、精度が210倍向上しました。これは、量子コンピューティングが実際の化学問題にすでに有用であることを示し、将来の創薬や材料科学研究を加速する可能性を秘めています。
詳細
背景と量子化学計算の重要性
化学、生物学、材料科学の分野では、分子や材料の特性を予測するために電子構造計算が不可欠です。しかし、原子数が増加し、分子システムが複雑になるにつれて、これらの計算は古典的なスーパーコンピューターでも指数関数的に困難になります。特に、タンパク質-リガンド複合体のような大規模な生体分子システムは、創薬において極めて重要ですが、その正確なシミュレーションは現在の計算能力の限界に挑戦し続けています。量子コンピューティングは、この「計算困難な問題」に対する新たなアプローチを提供し、これまで不可能だった規模と精度でのシミュレーションを可能にする潜在力を秘めています。
主要な成果:12,635原子タンパク質シミュレーション
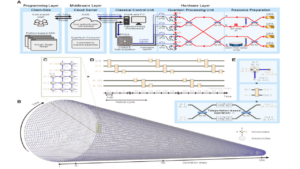
- 量子中心型スーパーコンピューティング(QCSC)フレームワーク: クリーブランドクリニック、理化学研究所、IBMの研究者たちは、IBMが提唱するQCSCフレームワークを活用しました。これは、古典的な高性能コンピューティング(HPC)と量子コンピューティングを緊密に統合し、それぞれの強みを最大限に引き出すハイブリッドアプローチです。
- 最大規模のタンパク質-リガンド複合体シミュレーション: 研究チームは、T4-リゾチームやトリプシンを含む12,635原子からなるタンパク質-リガンド複合体の電子構造をシミュレーションすることに成功しました。これは、これまでに量子技術を用いて行われた中で最大規模の化学計算であり、特に水溶液中という現実的な環境でのモデリングが重要です。
- 精度とスケールの飛躍的向上: このシミュレーションは、以前の同様の取り組みと比較して、システムサイズが40倍、ワークフローの精度が210倍という飛躍的な向上を達成しました。これは、単に量子ビット数を増やすだけでなく、ハイブリッドアルゴリズムの最適化と古典計算リソースの効率的な利用によって実現されました。具体的には、IBM Quantum Heron r2プロセッサの94量子ビットが使用されています。
産業・研究上の意味と展望
この画期的な成果は、量子コンピューティングがもはや理論的な可能性に留まらず、実際の化学問題において既に有用なツールとなりつつあることを明確に示しています。特に、医薬品開発、新素材科学、触媒設計といった分野において、分子シミュレーションのペースと精度を大幅に加速する可能性を秘めています。大規模なタンパク質系の正確なモデリングは、新薬の候補化合物のスクリーニング、作用機序の解明、副作用の予測などに直接貢献し、創薬プロセス全体の効率を劇的に向上させることが期待されます。この進展は、将来の耐障害性量子コンピューターが利用可能になった際に、さらに複雑な分子システムや量子化学の問題に対するブレークスルーを可能にするための重要な基盤を築くものとなるでしょう。
元記事: https://www.ibm.com/quantum/blog/cleveland-clinic-riken-chemistry







コメント