概要
「臨床AIレポート2026」の重要な調査結果によると、FDAによって承認された医療AIデバイスの95%が、単一の患者アウトカムも報告していません。これは、規制当局の承認と、現実世界での有効性および安全性のエビデンスとの間に重大なギャップがあることを示唆しています。報告書は、デジタルヘルスセンサーと統合されたAIツールを含め、AI医療機器の急速な普及と、不十分な市販後調査に対する懸念を提起しています。
詳細
医療AIデバイス普及と課題
医療分野における人工知能(AI)デバイスの導入は急速に進んでいますが、その実世界での効果と安全性に関する透明性は依然として不十分であることが、「臨床AIレポート2026」によって明らかにされました。特に衝撃的なのは、米国食品医薬品局(FDA)によって承認された医療AIデバイスの実に95%が、臨床現場における患者アウトカムのデータを一切報告していないという事実です。これは、イノベーションの推進と患者保護のバランスを取る上での重大な課題を浮き彫りにしています。
市販後監視の重要性と現状のギャップ
レポートは、デジタルヘルスセンサーと統合されたAIツールを含むAI医療機器の急速な普及に対して、適切な市販後監視が追いついていない現状に懸念を表明しています。承認段階での安全性・有効性評価は行われますが、実際の臨床現場で多様な患者集団に対して長期間使用された際の効果や潜在的なリスクを評価する「リアルワールドエビデンス」の収集が不足しています。AIの発展速度が包括的な評価プロセスを上回っていることが、このギャップの主な原因と見られています。
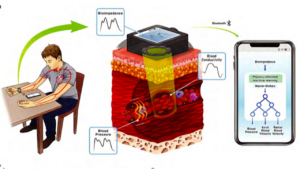
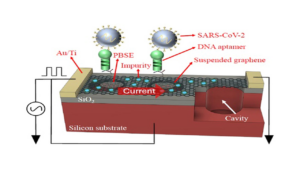
バイオセンサーとAIの未来への提言
この状況は、以下の緊急な対応が必要であることを示唆しています。
- 文書化の改善と透明性基準の強化
- 堅牢なガバナンスフレームワークの構築
- 厳格な市販後調査とデータ報告義務の導入
特にバイオセンサーを含むAI搭載医療デバイスが、患者に対して具体的な検証可能な利益をもたらすことを保証するためには、これらの取り組みが不可欠です。これにより、医療AI技術は真に患者中心のイノベーションとして機能し、医療の質と安全性を向上させる持続可能な発展を遂げることができるでしょう。将来的には、AIとバイオセンサーの統合がもたらす恩恵を最大化しつつ、そのリスクを最小限に抑えるための規制と評価の枠組みが求められます。
元記事: #







コメント