概要
この研究は、鉄ドープカーボンナノドット(FeCDs)のデュアルモード応答と機械学習を組み合わせたポータブルセンシングプラットフォームを提示しています。これは、キラルアスコルビン酸(L-AAとD-AA)のリアルタイム生体イメージングと差動検出を可能にします。複雑な生体環境でキラル異性体を選択的に認識し、その場でモニタリングすることは重要な分析課題でしたが、本プラットフォームはこの課題に対応します。機械学習アルゴリズムがFeCDsのユニークなデュアルモード応答を正確に解析します。
詳細
研究背景とキラル分子分析の課題
キラル分子は、左右対称ではない構造を持つ分子であり、その異なる異性体(エナンチオマー)は、生体システム内で全く異なる薬理活性や生理機能を示すことがあります。特にアスコルビン酸(ビタミンC)のキラル異性体であるL-AAとD-AAの選択的かつリアルタイムな検出は、食品科学、製薬、生物医学などの分野で重要な分析課題でした。複雑な生体環境下でこれらを区別する高感度かつ高選択的な手法が求められていました。
技術の核心と画期的な成果
本研究では、以下の要素を統合した、新しいポータブルセンシングプラットフォームが開発されました。
- 鉄ドープカーボンナノドット(FeCDs)のデュアルモード応答:蛍光と電気化学の両方で異なる応答を示します。
- 機械学習アルゴリズムによる信号解析:FeCDsのユニークなデュアルモード応答を正確に解析し、識別します。
- L-AAとD-AAの選択的識別と定量化:高感度かつ高選択的にキラル異性体を区別します。
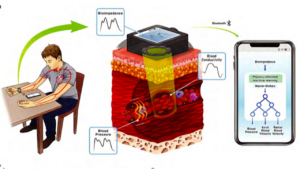
- スマートフォン連携によるポータビリティ:どこでもリアルタイムで分析が行える真のポータブルソリューションです。
このプラットフォームは、極めて高感度かつ高選択的にキラルアスコルビン酸異性体を識別し、定量化することを可能にしました。
影響と将来展望
この技術は、キラル分子の生体分析に革命をもたらす可能性を秘めています。特に、そのポータビリティとリアルタイム分析能力は、研究室環境外での現場診断や個別化医療において大きな進歩を意味します。例えば、患者の体内での特定の薬物動態のモニタリング、疾患バイオマーカーの早期検出、あるいは食品中の活性成分の品質管理など、幅広い応用が期待されます。機械学習とナノ材料の融合は、今後のバイオセンサー開発において、より複雑な生体情報を高精度で解析するための新たな道を開くでしょう。
元記事: #







コメント